近日,高明辉课题组在著名国际学术杂志《信号转导与靶向治疗》(Signal Transduction and Targeted Therapy)发表题为《LKB1-AMPK信号通路通过抑制脂肪酸合成而阻断铁死亡》(LKB1-AMPK Axis Negatively Regulates Ferroptosis by Inhibiting Fatty Acid Synthesis)的研究论文,揭示了LKB1-AMPK信号通路在调节铁坏死中的重要作用。
铁死亡(ferroptosis)是近年来发现的一种由铁依赖的氧化损伤引起的程序性细胞死亡形式,由一系列铁坏死诱导剂如erastin和RSL3引起。Erastin抑制谷氨酸/胱氨酸交换器xCT的活性,使细胞中半胱氨酸和谷胱甘肽(GSH)缺乏,进而破坏细胞氧化还原稳态,导致铁死亡的发生。谷胱甘肽过氧化物酶4(GPX4)是一种能清除脂质过氧化物的酶,其失活可以在不影响细胞内半胱氨酸和谷胱甘肽水平的情况下,导致铁死亡的发生。越来越多的证据表明,铁死亡与肿瘤、心脑血管疾病、神经退行性疾病等重大人类疾病息息相关。
葡萄糖和谷氨酰胺是细胞生存的必要营养物质。然而,本课题组的前期研究发现,谷氨酰胺对于细胞铁死亡也是必须的。谷氨酰胺通过线粒体代谢进入三羧酸循环,进而调控铁死亡的进程。类似地,葡萄糖进入细胞后经糖酵解途径和三羧酸循环途径产生ATP进而提供细胞的能量需求。但是葡萄糖是否调控铁死亡尚不清楚。
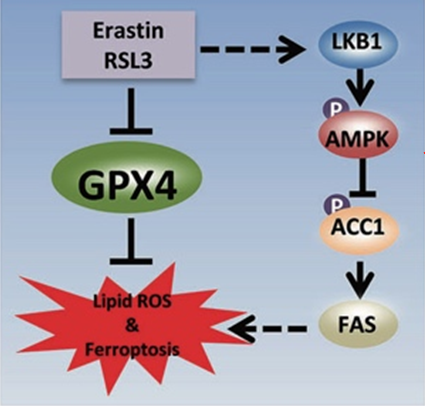
高明辉课题组发现葡萄糖的缺失可以抑制由erastin或RSL3诱导的铁死亡,表明葡萄糖对细胞铁死亡是必须的。AMPK是细胞的代谢和能量感受器。当葡萄糖缺乏时,细胞内AMP/ATP比值增加,进而激活AMPK。该研究发现激活AMPK能够抑制铁死亡的发生,而抑制AMPK能够促进铁死亡的发生。AMPK的上游激酶LKB1是一个非常关键的肿瘤抑制蛋白。LKB1在肺癌等肿瘤中突变频率非常高。该研究发现携带LKB1突变的非小细胞肺癌细胞对铁死亡异常敏感。这表明铁死亡诱导剂可能是携带LKB1突变的肿瘤的有效候选药物。该研究进一步发现当细胞受到铁死亡刺激时,AMPK被激活,进而磷酸化并抑制AMPK下游底物乙酰辅酶A羧化酶1(ACC1)的活性,以及抑制脂肪酸的合成,从而减缓脂质氧化物的积累和铁死亡的发生。
该研究是继高明辉课题组发现谷氨酰胺调控铁死亡之后(Gaoelal. MolecularCell 2015, 2019),在细胞营养代谢与铁死亡领域的另一重要发现。更重要的是该研究发现携带LKB1突变的肿瘤细胞对铁死亡刺激异常敏感,这为我们开发靶向携带LKB1突变基因的肿瘤的特异性药物奠定了理论基础。
哈工大生命科学中心高明辉研究员为本文的通讯作者,博士生李长炙为第一作者,硕士研究生董萱、石昕、陈康婕和博士后杜文静合作参与该项工作,康奈尔医学院博士张炜是该文章的共同通讯作者。该研究得到了国家自然科学基金,黑龙江省优秀青年基金和哈尔滨工业大学人才启动经费的支持。